La acumulación anómala de péptidos beta amiloide (Aβ) es una de las causas primeras en la Enfermedad de Alzheimer (EA). Sin embargo, mientras en la EA de desarrollo temprano y con componente genético, la acumulación de Aβ se debe principalmente a una inducción de sus síntesis, en la EA de aparición tardía (el 99% de los casos) se apunta a una eliminación defectuosa como la causante del aumento en los niveles del péptido. La célula tiene diferentes herramientas para la degradación de estas proteínas tóxicas, sin embargo, en la EA estos sistemas de eliminación se encuentran alterados.
Los factores responsables de estos defectos están aún por definir. Alteraciones similares se observan en la enfermedad de Niemann-Pick C (NPC), una afección neurológica que se caracteriza por una acumulación de colesterol y otros lípidos en los lisosomas, el orgánulo encargado de la eliminación de material intracelular. Además, diferentes estudios publicados previamente por la Dra. Anna Colell y por otros grupos muestran como el colesterol influye en la progresión de la EA, estimulando la síntesis y agregación de Aβ, así como su capacidad citotóxica.
En este trabajo, recientemente publicado en Autophagy, los investigadores analizaron el impacto del colesterol sobre la autofagia, el principal mecanismo celular de eliminación de agregados proteicos.
Mediante un modelo de ratones transgénico, los investigadores demuestran como el aumento de colesterol a nivel mitocondrial promueve la formación de vesículas autofágicas (autofagosomas). "Paradójicamente, esta inducción de autofagia no conduce a una mayor eliminación de Aβ: hay un enriquecimiento en colesterol en las membranas endolisosomales, lo que afecta a la fusión entre lisosomas y autofagosomas y por tanto, a la resolución del proceso autofágica ", explica Anna Colell. "La combinación de estas alteraciones no sólo impide una correcta degradación de Aβ, sino que favorece su secreción al medio extracelular contribuyendo a la aparición de los depósitos extracelulares del péptido", añade.
El tratamiento in vivo con un agente reductor de colesterol como la 2-hidroxipropil-β-ciclodextrina -su eficacia terapéutica está siendo evaluada positivamente para el tratamiento de la enfermedad de NPC- recupera el correcto funcionamiento de las vesículas autofágicas y hay una menor acumulación de Aβ en los autofagosomas.
"Estos resultados sugieren la utilización de inductores de autofagia en combinación con 2-hidroxipropil-β-ciclodextrina como una estrategia terapéutica para el tratamiento de la Enfermedad de Alzheimer", concluye la investigadora.
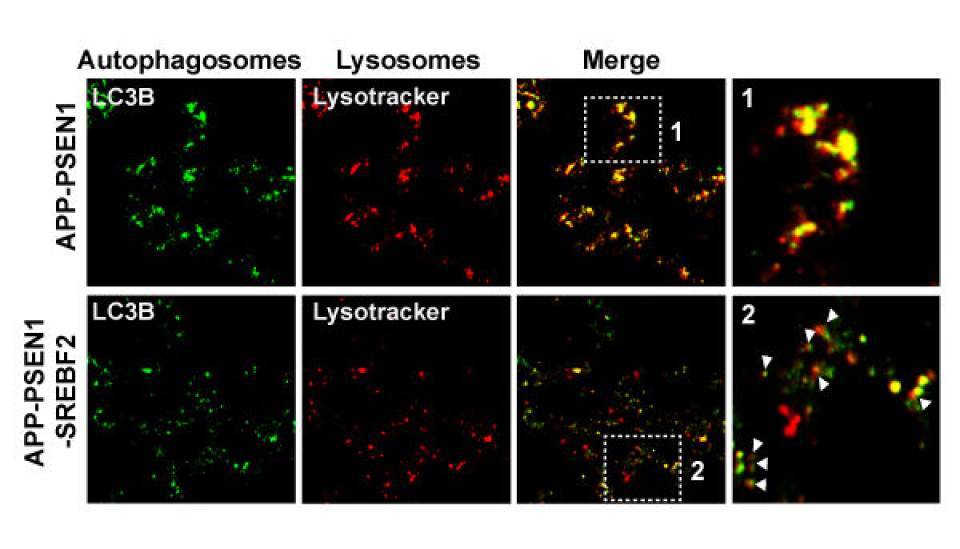
Información de la imagen: Fusión deficiente entre autofagosomas y lisosomas de ratones APP-PSEN1 que sobreexpresan SREBF2. La fusión entre autofagosomas (inmuno-teñidos con anticuerpo anti-LC3) y lisosomas (marcados con lysoTracker Red) se analizó mediante microscopía de fluorescencia. En el insert 1 se observa el solapamiento de los dos colores (en amarillo) que indicaría la fusión de los dos tipos de vesículas. Al insert 2 se observan las vesículas en alta proximidad pero sin fusionar (flechas blancas).
Referencia del artículo:
Cholesterol impairs autophagy-mediated clearance of amyloid beta while promoting its secretion Barbero-Camps E, Roca-Agujetas V, Bartolessis I, de Dios C, Fernández-Checa JC, Marí M, Morales A, Hartmann T, Colell A. Autophagy. 2018 Jun 4:1-26. doi: 10.1080/15548627.2018.1438807