La diabetes tipo 2 (DM2) y la obesidad están estrechamente ligadas. Un estudio llevado a cabo por investigadores del CIBERDEM y del IDIBAPS ha demostrado que la ausencia de la proteasa BACE2 (β-site APP-cleaving enzyme 2), una posible diana para la enfermedad de Alzheimer y de la DM2, empeora el fenotipo metabólico en ratones alimentados con una dieta obesogénica, rica en grasas.
En el estudio, dirigido por Joan-Marc Servitja y Anna Novials, del grupo de investigación del IDIBAPS Patogenia y prevención de la diabetes, también participaron el equipo de Mario Vallejo del Instituto de Investigaciones Biomédicas Alberto Sols, CSIC-UAM, y el grupo del IDIBAPS Control neuronal del metabolismo, que dirige Marc Claret. La primera autora es Daniela Díaz-Catalán, actualmente en el grupo de Trastornos endocrinos: interferencia entre determinantes moleculares, metabólicos y terapéuticos del IDIBAPS.
Las proteínas BACE1 y BACE2 pertenecen a una misma familia de proteasas que cortan péptidos de membrana. BACE1 se expresa en varios tejidos, incluido el cerebro, donde corta la proteína precursora de amiloide (APP), hecho que inicia la formación de los péptidos amiloide β presentes en las placas del cerebro de pacientes con la enfermedad de Alzheimer. Por este motivo, la inhibición farmacológica de BACE1 se ha propuesto como estrategia terapéutica para el tratamiento del alzhéimer. En cambio, BACE2 se halla en mayor abundancia en los islotes pancreáticos, donde inhibe la secreción de insulina de las células beta del páncreas.
Estudios previos del grupo demostraron que la ausencia de BACE2 recuperaba la secreción de insulina afectada por el efecto tóxico de la sobreexpresión de la hormona amilina humana en las células beta. Estos resultados llevaron a los investigadores a plantearse la posibilidad de que la inhibición de BACE2 podría ser una nueva estrategia para el tratamiento de la DM2. Para ello, sin embargo, era necesario comprobar las posibles consecuencias de la ausencia de BACE2 sobre el control del metabolismo. Con este fin, se administró una dieta rica en grasas, que induce alteraciones en el metabolismo, a dos grupos de ratones.
Los resultados indicaron que los roedores deficientes en BACE2 ganaron más peso que los ratones del grupo de control, no modificados. Este efecto iba precedido por una mayor ingesta de alimento y una alteración en las señales inhibitorias de la insulina y de la leptina en el hipotálamo. Además, los ratones deficientes en BACE2 presentaban niveles más altos de insulina en sangre y una mayor resistencia a la insulina inducidas por la dieta, evidentes antes de la aparición de la obesidad.
En resumen, el estudio demuestra que la supresión de BACE2 conlleva un mayor aumento de peso corporal, hiperfagia, hiperinsulinemia y resistencia a la insulina en ratones alimentados con una dieta obesogénica. Este hallazgo plantea la necesidad de reconsiderar el uso de inhibidores de BACE2 para el tratamiento de la diabetes, así como el uso de inhibidores de BACE1 para el tratamiento del alzhéimer, ya que la mayoría de dichos fármacos carecen de selectividad y también pueden inhibir la actividad de BACE2.
Este trabajo ha sido financiado por el Instituto de Salud Carlos III, cofinanciado por el Fondo Europeo de Desarrollo Regional (FEDER; Unión Europea, Una manera de hacer Europa) y por el CIBERDEM.
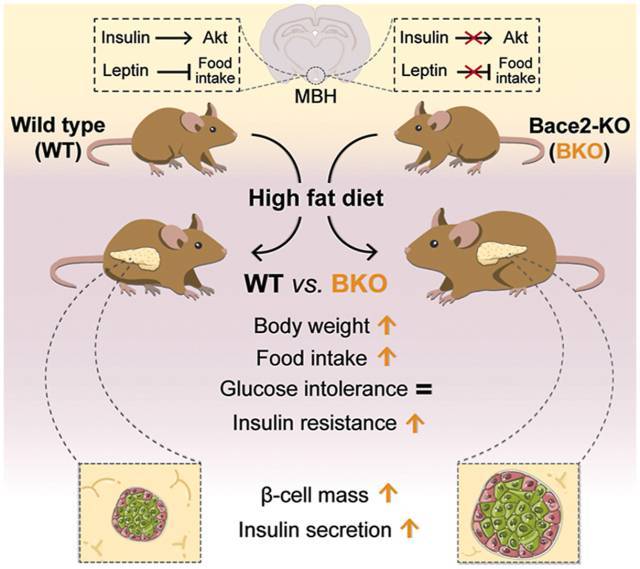
Resumen gráfico de los resultados de la investigación
Artículo de referencia
Díaz-Catalán D, Alcarraz-Vizán G, Castaño C, de Pablo S, Rodríguez-Comas J, Fernández-Pérez A, Vallejo M, Ramírez S, Claret M, Parrizas M, Novials A, Servitja JM. BACE2 suppression in mice aggravates the adverse metabolic consequences of an obesogenic diet. Mol. Metab.;53:101251 (2021). doi: 10.1016/j.molmet.2021.101251.
https://www.sciencedirect.com/science/article/pii/S221287782100096X?via%3Dihub




